澳银INSIGHTS|解锁生命密码,探索RNA疗法的无限可能

Figure 1:Katalin Karikó和Drew Weissman获得“2023年诺贝尔生理学或医学奖”。Source:诺奖官网
2023年10月2日,瑞典斯德哥尔摩卡罗林斯卡学院(Karolinska Institute)的诺贝尔大会宣布,将2023年诺贝尔生理学或医学奖授予美国科学家卡塔林·卡里科(Katalin Karikó)和德鲁·魏斯曼(Drew Weissman),因为发现了核苷酸基修饰而开发出有效的抗COVID-19 mRNA疫苗。Kariko和Weissmann开创性的发现了mRNA碱基修饰的重要性,使得mRNA疗法得以迅速应用至临床,根本上改变了对 mRNA 与免疫系统相互作用之间的理解。在现代人类健康面临的最大威胁之一期间,以前所未有的速度(从开发到上市仅用了一年时间)为疫苗研发做出贡献。因此将大众的视线再次聚焦到RNA疗法,一种极具潜力的治疗手段,目前正被广泛的开发和临床应用。而此前2006年,RNAi的两位先驱Andrew Fire和Craig Mello因1998年发表论文,确定双链RNA (dsRNA)是秀丽隐杆线虫(Caenorhabditis elegans)转录后基因沉默(PTGS)的病原体,这种现象称为RNA干扰(RNA interference, RNAi)而获得了诺贝尔生理学或医学奖。
RNA疗法是一种基于RNA水平的治疗方法,通过碱基配对与mRNA结合而影响mRNA的代谢过程(包括从前体mRNAs开始的剪接、mRNAs的运输、翻译和降解)。近10年来,RNA治疗在许多重要领域高度活跃,已成为治疗领域的研究热点。

图片来源:https://www.smgconferences.com/pharmaceuticals/uk/conference/rna-therapeutics
正文
众所周知,脱氧核糖核酸(deoxyribonucleic acid,DNA)和核糖核酸(ribonucleic acid,RNA)是生物细胞遗传物质的载体。在细胞中,根据中心法则DNA被转录成信使核糖核酸,而信使核糖核酸又被翻译成蛋白质,而蛋白质在调节生命活动中起着至关重要的作用。伴随分子生物学的快速发展,一些核酸被研究发现具有调控作用,例如:启动子、增强子、核酶、mRNA、miRNA、siRNA等。针对不同类别功能、作用机制进行的核酸新药研发日益成为当前新药开发的热门赛道。
与传统小分子化学药物和抗体类药物不同,核酸药物高度以来碱基互补配对原则参与基因转录和翻译的过程,可高效特异性调控致病靶基因或靶RNA。此外,核酸药物具有治疗效率高、药物毒性小、特异性强、应用领域广泛等优势,有望成为在小分子化药、抗体后出现的第三类重磅药物,具有广阔的研发和应用前景。
与基于DNA的疗法相比,基于RNA的疗法因其独特的理化性质和特征更具前瞻性。RNA可在DNA、RNA、蛋白质,三种生物大分子中发挥作用。RNA分子(例如:ASO、siRNA、miRNA)可直接通过碱基互补配对靶向mRNA和ncRNA。理论上说,RNA可通过选择正确的核苷酸序列靶向任何基因。人类基因组中大多DNA序列都已完成了非编码转录被,而已获批的蛋白质水平的靶向疗法(即小分子化药和抗体药物)只能对0.05%的人类基因组进行药物治疗。85%的蛋白质不能和小分子化药进行靶向结合。体外转录(IVT)mRNA可在进入细胞质后用于蛋白质替代治疗或免疫,并不会像DNA疗法那样发生不可逆转的基因组变化、诱发遗传风险。此外,通过CRISPR基因组编辑可以直接修改目标RNA序列治疗特定疾病。RNA aptamers可阻断蛋白质活性,作用过程类似小分子抑制剂和抗体。因此,RNA疗法可以拓宽药物靶点的范围这一优势,使得其成为最具吸引力的治疗方式。
关于RNA疗法的基础研发最早可追溯至1956年(Figure 1),Rich和Davies发表了第一个核酸杂交反应,证明RNA可以基于其碱基配对中的相同互补性形成与DNA相似的构型。这一发现为随后1993年发现miRNA(micro RNA)和1998年发现RNA interference奠定了基础,并指出RNA双链体的产生是RNA沉默的关键步骤。
1998年首款基于RNA疗法的药物Vitravene (Fomivirsen)中文名福米韦生,是FDA批准上市的第一个反义寡核苷酸类药物,于1999年获得EMA批准上市,由Isis Pharmaceuticals和Novartis联合研发。该药物由21个硫代脱氧核苷酸组成,主要用于治疗艾滋病(AIDS)病人并发的巨细胞病毒(CMV)性视网膜炎。通过对人类巨细胞病毒(CMV) mRNA的反义抑制发挥特异抗病毒作用;疗效维持久,给药次数少,不良反应轻。上市初期,市场对于抗巨细胞病毒药物的需求甚为迫切;随后由于高活性抗逆转录病毒疗法的发展,巨细胞病毒病例数量急剧下降。该药在欧洲和美国分别于2002年和2006年退市。
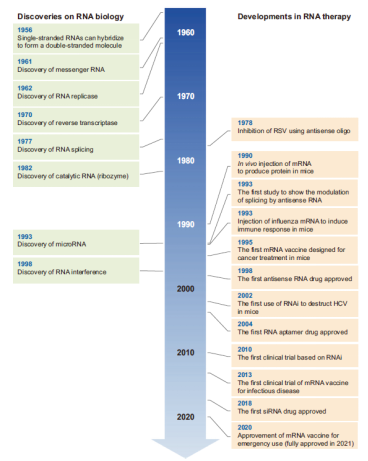
Figure 1. The historical timeline of important discoveries in RNA biology and key developments in RNA therapy. Source: Kim YK. RNA therapy: rich history, various applications and unlimited future prospects. Exp Mol Med. 2022 Apr;54(4):455-465. doi: 10.1038/s12276-022-00757-5. Epub 2022 Apr 19. PMID: 35440755; PMCID: PMC9016686.
RNA大分子具有很多功能,可以简单分为coding或messenger RNA(mRNA)和non-coding RNA(ncRNA)。
【而ncRNA包括ribosomal RNA(rRNA)、transfer RNA(tRNA)、small nuclear(snRNA)、small nucleolar RNA(snoRNA)、long non-coding RNA(lncRNA)、short hairpin RNA(shRNA)、micro-RNA(miRNA)、transfer messenger RNA(tmRNA)、small interfering RNA(siRNA)、small activating RNA(saRNA)、piwi-interacting RNA(piRNA)、circular RNA(circRNA)、ribozymes和exosomal RNA。】
细胞内具体的位置和不同类型的RNA详见Figure 2.
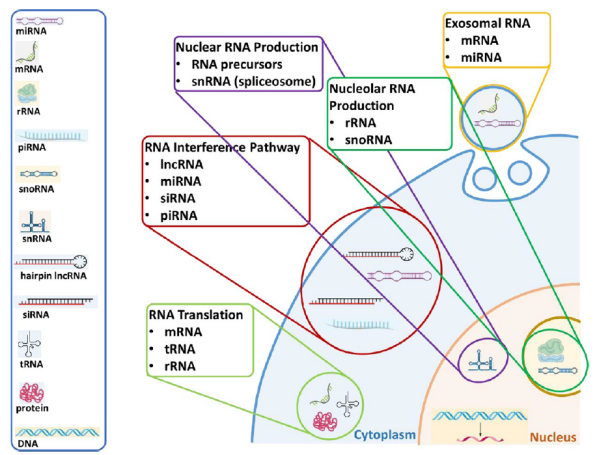
Figure 2 .Types of naturally occurring RNA and their cellular functions and localizations. Source:Sasso JM, Ambrose BJB, Tenchov R, Datta RS, Basel MT, DeLong RK, Zhou QA. The Progress and Promise of RNA Medicine─An Arsenal of Targeted Treatments. J Med Chem. 2022 May 26;65(10):6975-7015. doi: 10.1021/acs.jmedchem.2c00024. Epub 2022 May 9. PMID: 35533054; PMCID: PMC9115888.
RNA疗法的工作方式如下图所示,作用机理主要是通过寡核苷酸与mRNA通过碱基互补配对原则结合,进而干扰影响mRNA的代谢过程实现治疗目的。
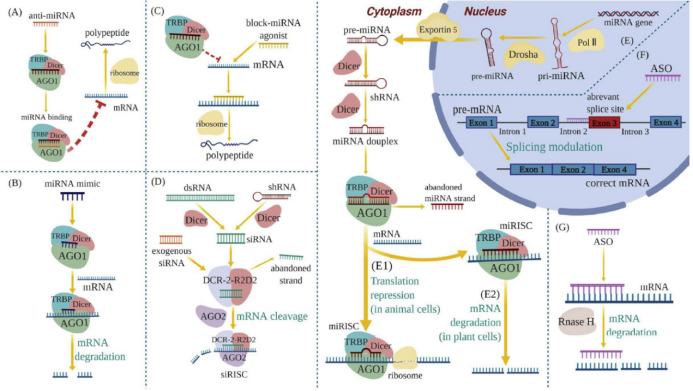
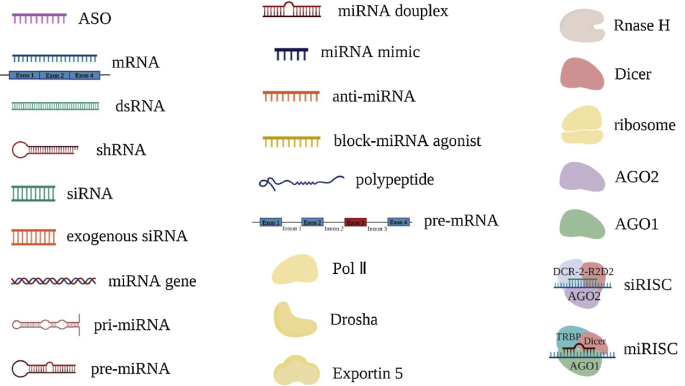
Figure 3. Mechanisms of RNA therapeutics.Source:Liang X, Li D, Leng S, Zhu X. RNA-based pharmacotherapy for tumors: From bench to clinic and back. Biomed Pharmacother. 2020 May;125:109997. doi: 10.1016/j.biopha.2020.109997. Epub 2020 Feb 13. PMID: 32062550.
(A)反义miRNA与目标miRNA的活性链互补,从而削弱内源性miRNAs的基因沉默效应,进而促进蛋白质的表达。
(B)增强内源性miRNAs的功能,减少细胞内蛋白的表达。
(C)阻断miRNA激动剂其被用来阻止RISC与特定的mRNAs结合,从而“阻断”miRNA结合部位,以增加相关蛋白质的表达。
通常,RNA疗法是通过利用细胞内的RNase H(G)或形成RNA诱导的沉默复合体(RISC)(D、E1、E2)来切割靶基因。在植物细胞中,miRNA与目标mRNA完全结合以降解(E1),而在动物细胞中,因其不能与其目标mRNA互补,后者阻止核糖体并减少翻译(E2)。ASO能够调节mRNA(F)的剪接过程。它通过与异常的mRNA剪接位点结合来纠正错误的剪接。

而根据不同类型的RNA药物,下表展示了几种其具体的作用机制和作用靶点。
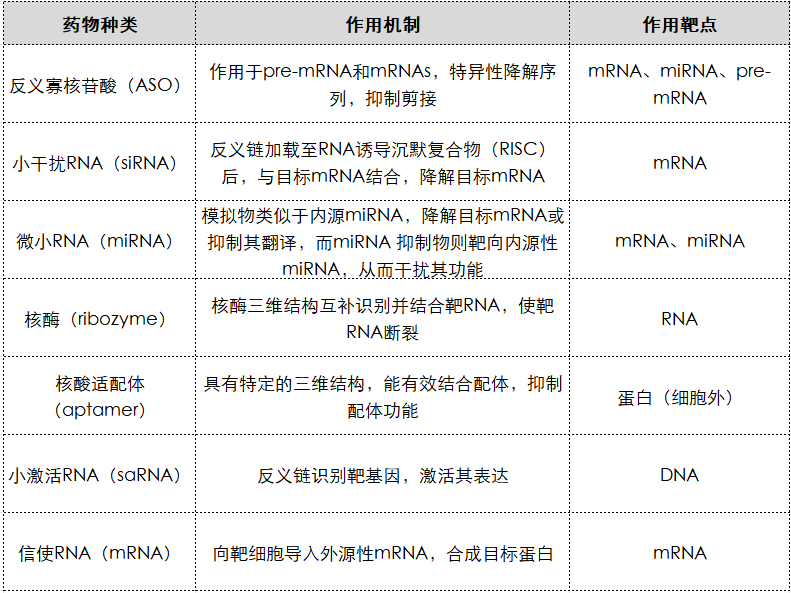
Chart 1:RNA药物种类及作用机制。Source:裴佳伟,王雪,黄倩,谭慎行,田野*,骞爱荣*. 小RNA合成技术与小RNA药物研究进展.
陕西师范大学学报(自然科学版). 2023, 51(3): 1-15 https://doi.org/10.15983/j.cnki.jsnu.2023201
由此,RNA疗法的研发主要聚焦在两方面:一是反义RNA(antisense RNA),短寡核苷酸识别并与内源性RNA转录本中的互补序列杂交,从而进行改变。二是信使RNA(mRNA,messenger RNA),其编码某些肽或蛋白质的mRNA在细胞质中引发其短暂表达(例如,用于替代缺陷蛋白或提供疫苗抗原)。
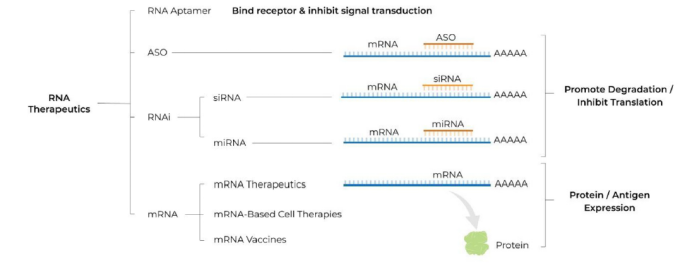
Figure 4. Schematic illustrating different classes of RNA therapeutics. ASO, antisense oligonucleotide; RNA, ribonucleic acid; RNAi, RNA interference; siRNA,
small interfering RNA; miRNA, microRNA; mRNA, messenger RNA; A, adenosine molecule; AAAAA, poly A tail. Source: Damase TR, Sukhovershin R, Boada C, Taraballi F, Pettigrew RI, Cooke JP. The Limitless Future of RNA Therapeutics. Front Bioeng Biotechnol. 2021 Mar 18;9:628137. doi: 10.3389/fbioe.2021.628137. PMID: 33816449; PMCID: PMC8012680.
伴随RNA生物学、生物信息学的发展,促使了RNA疗法的快速发展,并展现了如下驱动其快速发展的优势,诸如:RNA疗法具有可针对小分子化药不能靶向的靶点进行结合;与小分子和重组蛋白相比,可快速成本低廉的方式进行研发;可快速改变mRNA的结构序列用于个人精准化治疗适应不断变化更新的病原体。
-①-
RNA疗法
5大优势归纳



-②-
RNA疗法的几种类型
将其分为4种类型的疗法进行详细描述

已上市药物详见图表:
全球已上市及申请上市的RNA药物
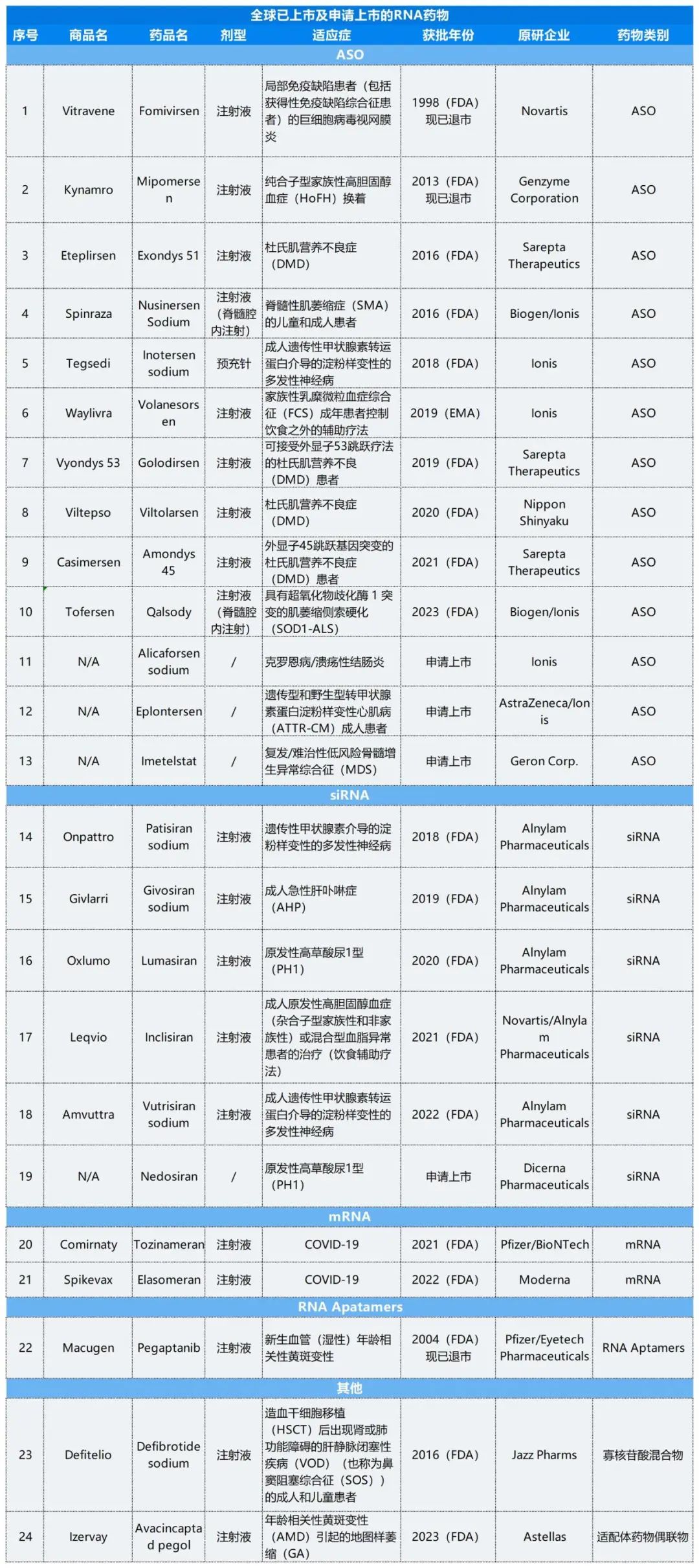
Chart 2:全球已上市及申请上市的RNA药物。
Source:智慧芽数据库,数据截止:2023年9月28日。
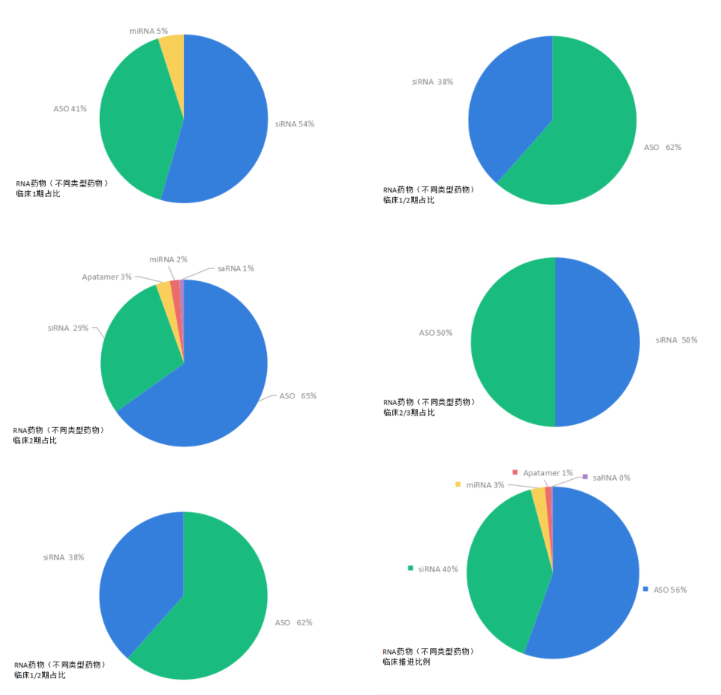
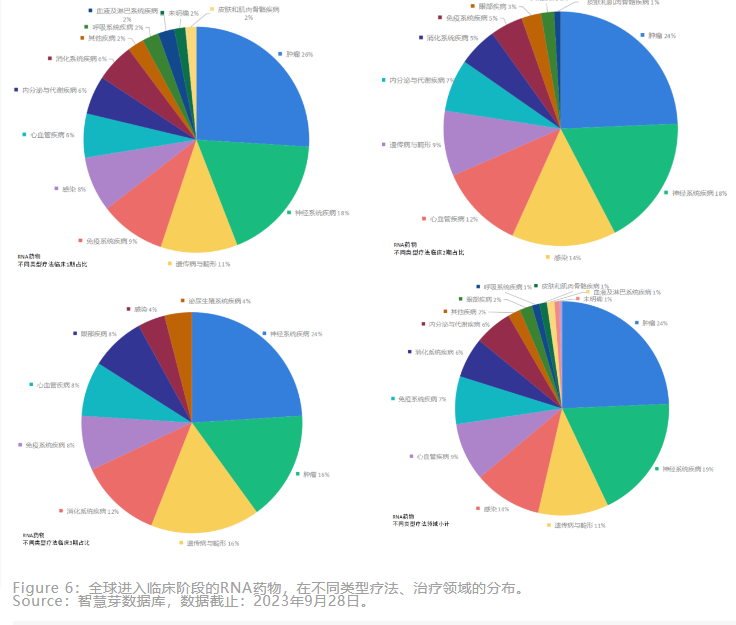
RNA疗法的研发生产一般流程为:测序、靶点确定、序列设计和优化、递送技术研究、核酸合成、纯化、制剂及生产等。在研发过程主要需要克服以下三方面的障碍:
(1)组织中广泛存在的核酸酶会快速降解外源RNA;(2)将带负电的RNA传递通过疏水性的细胞膜;(3)外源RNA具有强烈的免疫原性,会导致细胞毒性并损害影响其翻译转化为治疗性蛋白质。
根据沙利文2022年5月发表的报告提到,小核酸药物(即本文所指ASO、siRNA、miRNA、Aptamer)研发过程中,在药效学、药代动力学、CMC、递送等方面遇到瓶颈。包括:递送效率低、靶向性差、脱靶毒性、免疫介导毒性、组织/细胞穿透性低、化学修饰方法严格、规模化生产难度高。对于mRNA产品研发,仍需解决mRNA设计方面的序列优化和核苷修饰技术的优化、提高体内表达蛋白质效率、高效安全递送、提高mRNA纯度、确保颗粒大小一致性、提高大规模生产时的包封效率,确保产品稳定并降低成本等。
针对研发过程中遇到的问题,需要以相应的技术路径解决。
在设计方面,需要准确获取致病基因的功能信息,有针对性的进行序列设计;在修饰方面,利用特定化学修饰方法优化结构,提高血清稳定性、降低毒性;
在合成方面,针对市场潜力大的产品进行液相合成技术研究,发展小核酸单体合成技术和发酵技术,保证产品质量并实现商业化收益;在制剂方面,通过复合药物开发、沉默多个信号通路的靶点,实现多靶点调控,提升药物疗效。
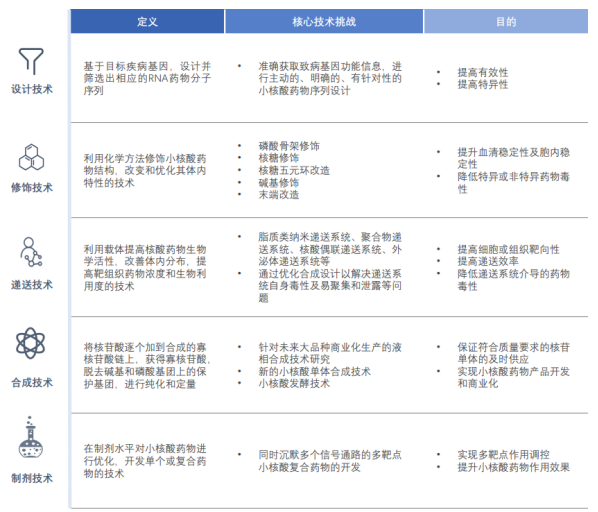
Figure 7.小核酸药物核心研发技术挑战。Source:沙利文:核酸药物市场产业现状与未来发展报告。
值得一提的是,核酸设计和制备工艺目前相对成熟,而向人体各组织细胞中递送药物是发挥其治疗功能的关键,也是RNA疗法面临的技术难点之一。目前递送过程中主要存在的难点包括:(1)核酸不稳定性,易于被血浆、组织中核糖核酸酶降解,被肝脏和肾脏快速清除;
(2)核酸自身免疫原性易被免疫系统识别;(3)药物靶向性差;
(4)核酸分子量大且带负电荷使其不易跨过细胞膜进入细胞质;
(5)在体内无法释放。针对上述这些难点,RNA疗法将重点聚焦了核酸分子改造、药物递送载体、偶联技术等方向的研究并提供多种解决思路。
对核酸分子进行改造,包括mRNA结构元件的设计和核酸分子的化学修饰两种方式,从而提高其稳定性增加翻译效率,延长半衰期。例如首个上市ASO药物Fomivirsen就是采用的硫代磷酸酯进行修饰。Alnylam公司开发的siRNA药物GIvosiran采用了核糖修饰的方法。药物递送以脂质体为代表应用为代表,其中尤以脂质纳米粒(LNP)最为受到头部公司诸如Moderna、Curevac公司应用最为广泛。但LNP递送存在一些缺点,例如mRNA递送时体内逃逸率低、LNP分子量大易引起过敏反应、LNP递送通常靶向肝脏限制适用范围、LNP易氧化降解、制备重现率差等。因此斯微生物采用了LPP等不同材料进行递送、此外外泌体递送因无免疫排斥、能够穿透血脑屏障的优势具有极大的应用潜力。采用生物偶联技术可促进细胞摄取、增强传递效率。主要应用N-乙酰半乳糖胺(GalNAc)与肝脏细胞表面去唾液核糖蛋白受体结合,通过与小核酸药物形成缀合物,实现药物靶向递送并迅速内化,大幅度提升药物安全性、减少脱靶效应增强药效。2019年获批的Givlaari是首个使用GalNAc递送技术上市的RNA疗法药物。
基于RNA疗法的用药优势和广泛应用前景,近年来资本的关注,根据Nature发表的《RNA therapeutics on the rise》文章中提到RNA疗法相关公司融资额近年来迅速增加。2015年至2020年,上市寡核苷酸公司市值增长94.2%。自2015年以来,三家具有代表性的mRNA治疗公司(Moderna Therapeutics、BioNtech和CureVac)吸引了28亿美元的私人投资。其中Moderna创造了2018年规模最大的生物技术IPO,市值约为76亿美元。自2017年以来,RNA相关的小分子公司已经筹集了大量投资,包括那些直接针对RNA的公司(向Arrakis、Expansion、Skyhawk和Ribometrix提供了2.62亿美元资金),以及针对表位转录组学相关蛋白质的公司(向Accent、Storm、Gotham和Twentye-Seven Therapeutics提供了1.94亿美元资金)。
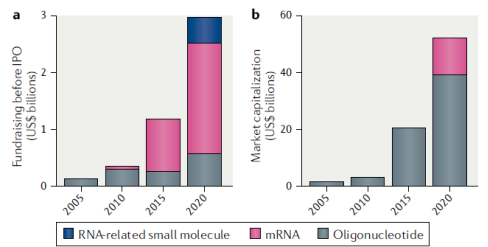
Figure 8. RNA疗法近15年一、二级融资概览。Source:RNA therapeutics on the rise, 27 April 2020,Nature Reviews Drug Discovery 19, 441-442 (2020),doi:
Figure 9. RNA疗法领域重要企业及相关合作企业。Source:杨若南,许丽,徐萍,等.RNA疗法产业发展态势分析及建议[J].中国生物工程杂志, 2021, 41(2):10.DOI:10.13523/j.cb.2009037.
RNA疗法领先的生物技术公司除获得资本助力外,许多MNC公司同样通过合作研发持续布局,例如由华人科学家何川(Chuan He)教授与Howard Chang教授等人于2018年共同创立Accent Therapeutics,于2020年与AstraZeneca宣布达成了一项价值达11亿美元的合作,双方将合作开发靶向RNA修饰蛋白(RMPs)的转化疗法来治疗多种癌症,并将这种疗法商业化。根据合作协议条款,Accent Therapeutics将负责该项目的临床前研发,直至一期临床试验结束。由AZ主导后续研发和商业化活动 。Accent Therapeutics将获得5500万美元的预付款,并在项目中以期权和里程碑付款的形式获得最高11亿美元的资金,以及在净销售额中获取5%或10%~20%的特许权使用费。
目前RNA疗法通过获批上市证实可应用至罕见病,特别关注神经系统疾病和肝脏疾病,多数属于孤儿药。而美国、欧盟对罕见病药物支付体系的建立与完善吸引了众多资本入局,力求寻找新的增长点。而国内RNA疗法产业处于起步阶段,同时对孤儿药领域开发仍存在政策提升的空间。亟待加强对罕见病研究的研发支持和绿色通道建立。重点突破科研领域中药物稳定性、免疫原性、靶向性、药物体内逃逸率等问题。
RNA疗法毋庸置疑已受到广泛的,不论生物技术企业还是资本市场的注意,随着核酸稳定性增强技术和递送技术的成熟,相信未来会有更多RNA疗法的药物从临床走向应用。但整体RNA疗法在体内除肝脏以外的器官中递送,仍有难点。未来将在多器官靶向方面,突破现有靶向肝脏限制,通过加强生物膜结构和调控规律的研究,提高递送的准确性、进一步提升RNA疗法的药效,监控长期安全性问题。此外,在储存和运输的稳定性方面仍需要持续把控和降低成本。
番外小故事~
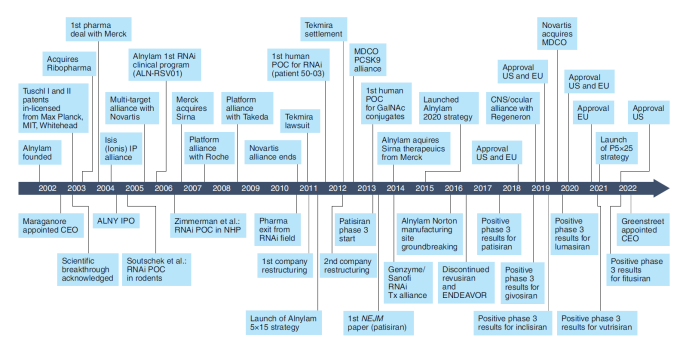
全球小核酸药物领军企业Alnylam Pharmaceuticals的离任CEO John Maraganore博士于2022年在Nature发表的《Refections on Alnylam》文章中,回顾在职19年期间企业起起伏伏的发展情况时所提到的,RNA治疗的前景是美好的,但除了技术本身应用的障碍外,公司如何通过IP荆棘丛、完善递送技术、打造强有力的管线、同时保证充足的资金供给同样是一个基于RNA技术的创新型公司需要持续学习并始终报以理性的激情。
尤其在2010年9月RNA技术遭Novartis和Roche的投资冷遇,2011年初New York Times的Andrew Pollack发表题为《“Drugmakers”Fever for the Power of RNA Interference Has Cooled.》,外界对RNAi的看法急转直下的时候,John仍坚定不移坚守RNA疗法,专注打造最优递送的临床管线。在2011年JPM会议中提出新战略“Alnylam 5×15”计划,承诺2015年底前推进5个RNAi药物进入临床阶段。虽然此举也曾遭到团队的质疑,但是结果证明了这一目标的正确。
在2015年底,成功推进了8个项目进入临床。在随后的临床管线推进中,一方面证实了RNAi疗法不仅可应用至罕见病,更可以治疗患者群体更多的适应症,成为了全新的药物类型。同时解决了曾经不可成药的靶点上,成药性的潜力问题,在治疗疾病方面也具备了良好的风险收益比。
2018年Patisiran(商品名:Onpattro)获批上市,证明了Alnylam这个阿拉伯语“一串珍珠”的猎户座腰带中央恒星以信仰闪耀的创新公司商业化的能力。成为了现如今拥有超过1600名员工,累计融资77亿美元的上市公司。
在此引用Nature原文文首中提到的萧伯纳的名言:
The reasonable man adapts himself to the world; the unreasonable one persists in trying to adapt the world to himself. Therefore, all progress depends on the unreasonable man.
“对于当下身处困境中的医药行业来说,更加值得思考。”

Who's John Maraganore
John Maraganore博士出生于芝加哥。2002年至2021年期间担任Alnylam公司的创始人兼首席执行官和董事,创立并领导公司完成了从RNA干扰药物(RNAi)的早期平台研究开始、到临床开发、并在全球获得了世界上前四个RNA干扰药品ONPATTRO®、GIVLAARI®、OXLUMO®和Leqvio®的注册批准和商业化的历程。在Alnylam,他还领导了公司的价值创造战略,创造了250亿美元的市值,包括20多个重要战略合作。

